Des Nanoparticules pour l'imagerie du Cancer
Une des voies de ciblage proposées par les nanotechnologies est l'utilisation des nanoparticules, de nombreux travaux ont montré l’intérêt que pouvait présenter leur utilisation dans le domaine médical, en particulier comme agents de contraste dans le domaine de l’imagerie. Il est en effet possible de concevoir des nanoparticules qui permettent simultanément de visualiser et de traiter certaines tumeurs. Une fois à l’intérieur de la cellule, les nanoparticules peuvent agir comme un puissant agent de contraste qui permet de localiser la tumeur par IRM. Le traitement quant à lui repose sur l’exploitation des propriétés physico-chimiques de la tumeur.
Les nanoparticules de silice
Depuis plusieurs années, les scientifiques explorent la possibilité d'utiliser des nanoparticules capables de circuler dans le corps humain comme outils de diagnostic et de traitement du cancer. Mais la toxicité de la plupart des structures étudiées constitue un obstacle majeur pour leur application chez l'homme. Des chercheurs sont donc parvenus à fabriquer une nanoparticule luminescente, biodégradable et aux effets secondaires minimes pour une utilisation plus sûre en médecine. C'est la nanoparticule de silice.
Le silicium se présente comme un matériau intéressant, en effet, trois caractéristiques composant le silicium poreux, lui confèrent un avantage primordial pour une utilisation en médecine : il est bien toléré par l'organisme humain (biocompatible), il s'y dégrade progressivement et possède une luminescence qui lui est propre, donc détectable.
La propriété de luminescence est essentielle, à la fois pour les applications en imagerie médicale et pour le suivi du déplacement in vivo d'éventuelles molécules thérapeutiques qui seraient incluse dans la nanoparticule de silice (médicaments) , ainsi que pour le suivi de cellules cancéreuses qui pourraient migrer (tumeurs). Dans les autres formes de nanoparticules développées, la propriété de luminescence est le plus souvent assurée par l'addition de produits chimiques organiques toxiques, ou par l'intermédiaire de nanocristaux semi-conducteurs. Cela peut entrainer une accumulation dans le corps - notamment au niveau du foie - de métaux lourds et dangereux (car parfois toxiques), comme nous l'avons vu pour les Quantum Dots.
Par contraste, le silicium existe déjà sous forme d'oligoélément chez l'homme, c'est à dire une classe de nutriments minéraux purs nécessaires à la vie d'un organisme mais en quantités très faibles. Un des produits de dégradation du silicium poreux, l'acide orthosilicique, se trouve naturellement dans de nombreux tissus, les nanoparticules de silice peuvent donc être biodégradées. Enfin, l'acide silicique est évacué de façon efficace dans les urines, permettant ainsi d'évacuer la silice introduite dans l'organisme.
Quant à la troisième qualité du silicium poreux, également indispensable dans l'application des nanotechnologies dans le ciblage du cancer, c'est que sa biodégradation s'effectue relativement lentement, en effet la nanoparticule doit pouvoir se maintenir dans le système sanguin pendant plus de deux heures étant donné que si elle est éliminée par le foie ou les reins, elle ne peut pas atteindre la tumeur.
D'une taille de 100 nanomètres, la nanoparticule de silice est plus grande que la plupart de celles créées à ce jour pour le transport de médicaments dans le flux sanguin. Ces dimensions permettent le changement de plus grandes quantités de molécules thérapeutiques, ce qui devrait contribuer à l'efficacité du dispositif. C'est également un facteur de sécurité puisque la dégradation naturelle de la nanoparticule en fragments qui peuvent être éliminés par l'intermédiaire des reins est largement possible. Des essais préliminaires effectués sur des souris traitées avec ces nouvelles nanoparticules n'ont pas mis en évidence des modifications à long terme des organes de désintoxication que sont le foie, la rate et les reins. L'utilisation de cette méthode est donc prometteuse.
Pour mieux pouvoir cibler les cellules tumorales, des chercheurs sont parvenus à fabriquer des fluorophores biphotoniques capables d'absorber deux photons dans le proche infra-rouge et permettant donc une détection plus précise. Ces fluorophores sont ensuite encapsulés dans les nanoparticules de silice poreuses pour permettre leur circulation en milieu biologique. L’originalité de ce travail réside dans le fait que, contrairement aux longueurs d’onde ultraviolettes, les longueurs d’onde infrarouges pénètrent plus profondément dans les tissus et sont moins énergétiques, ce qui a pour avantage d’explorer plus profondément les tumeurs sans pour autant endommager les tissus. De plus, l’utilisation de fluorophores biphotoniques favorise l’accès à une résolution spatiale en 3D, permettant de détecter et de traiter de façon encore plus précise les cellules tumorales. L’une des voies envisagées serait d’encapsuler dans les pores des nanoparticules de silice, outre l’agent fluorescent, des médicaments capables de traiter localement la cellule cancéreuse.
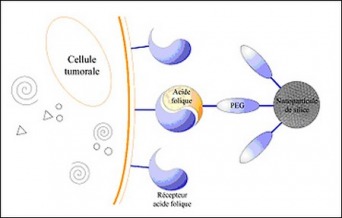
Cependant encore faut il que ces nanoparticules de silice se fixent au cellules cancéreuses, on greffe donc sur les nanoparticules des éléments de reconnaissance de certaines tumeurs, comme l'acide folique, reconnu par les cellules du cancer du col de l'utérus ou du cancer du sein. Plusieurs molécules pourraient être greffées pour permettre la détection d'autres tumeurs. Cette technique est également utilisée pour diriger les médicaments encapsulés dans les nanoparticules vers les tumeurs. C'est la véctorisation des médicaments.
Les nanoparticules magnétiques
Les nanoparticules magnétiques sont des nanoparticules composées d'un cœur en fer
dur et créées pour se fixer sélectivement sur une tumeur ( en particulier sur des zones qui ont résisté à la radiothérapie). Leurs propriétés magnétiques sont d'une grande utilité. en effet, ces propriétés leur confèrent des caractéristiques additionnelles par rapport aux nanoparticules habituelles biodégradable en silice. On peut donc parler d'une double action dans leur utilisation.
Structure de la nanoparticule
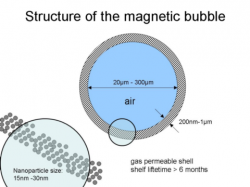
On peut voir sur cette image la structure d'un autre genre de nanoparticule magnétique, à cœur creux cette fois. La "coque" de fer d'épaiseur variant entre200 nanomètres et 1 micromètre.
Leur utilisation principale réside dans l'imagerie biologique. En effet, leur propriétés magnétiques permettent d'être en total adéquation avec certaines techniques de scannage. Pour l'imagerie du cancer, leur accumulation dans la tumeur permet une meilleure visualisation de celle-ci par les IRM ( Imagerie par Résonance Magnétique ), rendant ainsi le traitement plus précis. Leur rôle dans ce cas là est donc de servir "d'amplificateur" d'une l'image, afin que sa netteté permette un diagnostic ou un détection de cellules spécifiques beaucoup plus efficaces et donc fiables.
Un moyen pour que ces nanoparticules magnétiques arrivent à la tumeur est de se faire transporter par des agents de l'organisme. En effet des nanoparticules d'oxyde de fer peuvent être associées à des agents biologiques spécifiquement dirigés contre les cellules cancéreuses, comme les anticorps, qui peuvent les conduire directement vers les cellules tumorales. Les nanoparticules de fer sont en fait enrobés d'une substance qui sera détectée comme étrangère à l'organisme (le choix des substances est grand) , donc comme parasite. La réaction immune du corps ne se fera pas attendre, et les anticorps viendront ingérer ces nanoparticules. Les agents biologiques immuns serviront en quelque sorte de taxi aux nanoparticules magnétiques, qui pourront donc rejoindre les cellules cancéreuses.
Mais ici encore, leurs propriétés magnétiques vont être utiles. En effet, si les nanoparticules magnétiques ne sont pas correctement acheminés jusque la tumeur, il est possible de les rapprocher ou même les mettre en contact avec cette dernière. Cela est possible grâce à la présence d'un champ magnétique adapté à ces nanoparticules, qui va être réglé à la bonne intensité afin de ne pas perforer les tissus internes, et qui dirigera les petites boules de fer jusque l'endroit voulu. Une grande précision et une minutie énorme sont donc exigés. Cette manipulation est en général effectuée par des robots.
Les nanoparticules magnétiques seraient donc un très bon moyen de cibler les tumeurs et de les situer, tout en améliorant la qualité des IRM.
Cependant, quelques petits inconvénients font vite surface, et mettent terme au prestige des ces nanoparticules magnétiques. En effet, elles ont déjà été testées par beaucoup d'équipes de recherche mais les résultats (même si ceux-ci sont très prometteurs), sont toujours limités par les faibles performances magnétiques des matériaux utilisés, généralement des oxydes. La régulation d'un champ magnétique adapté reste donc très difficile à mettre en place. Un autre problème réside dans le fait que ces nanoparticules, étant composées de fer, sont bien sûr oxydables, et ne sont pas biodégradables. Si leur élimination n'est pas faite par la voie de l'urine ou autre, elles risquent donc de rester dans l'organisme, et ce, pendant une durée indéterminée. Les effets secondaires sont encore mal connus.
Des chercheurs proposent donc de synthétiser des nanoparticules de fer pur aux propriétés magnétiques innovantes, de développer un nouvel enrobage pouvant les protéger de l'oxydation et d'assurer leur ciblage vers certaines cellules tumorales. Le défi est d'obtenir pour ces nanoparticules une forte sélectivité pour les différentes tumeurs et une grande efficacité préservée tout au long du traitement.
Un moyen pour que ces nanoparticules magnétiques arrivent à la tumeur est de se faire transporter par des agents de l'organisme. En effet des nanoparticules d'oxyde de fer peuvent être associées à des agents biologiques spécifiquement dirigés contre les cellules cancéreuses, comme les anticorps, qui peuvent les conduire directement vers les cellules tumorales. Les nanoparticules de fer sont en fait enrobés d'une substance qui sera détectée comme étrangère à l'organisme (le choix des substances est grand) , donc comme parasite. La réaction immune du corps ne se fera pas attendre, et les anticorps viendront ingérer ces nanoparticules. Les agents biologiques immuns serviront en quelque sorte de taxi aux nanoparticules magnétiques, qui pourront donc rejoindre les cellules cancéreuses.
Mais ici encore, leurs propriétés magnétiques vont être utiles. En effet, si les nanoparticules magnétiques ne sont pas correctement acheminés jusque la tumeur, il est possible de les rapprocher ou même les mettre en contact avec cette dernière. Cela est possible grâce à la présence d'un champ magnétique adapté à ces nanoparticules, qui va être réglé à la bonne intensité afin de ne pas perforer les tissus internes, et qui dirigera les petites boules de fer jusque l'endroit voulu. Une grande précision et une minutie énorme sont donc exigés. Cette manipulation est en général effectuée par des robots.
Les nanoparticules magnétiques seraient donc un très bon moyen de cibler les tumeurs et de les situer, tout en améliorant la qualité des IRM.
Cependant, quelques petits inconvénients font vite surface, et mettent terme au prestige des ces nanoparticules magnétiques. En effet, elles ont déjà été testées par beaucoup d'équipes de recherche mais les résultats (même si ceux-ci sont très prometteurs), sont toujours limités par les faibles performances magnétiques des matériaux utilisés, généralement des oxydes. La régulation d'un champ magnétique adapté reste donc très difficile à mettre en place. Un autre problème réside dans le fait que ces nanoparticules, étant composées de fer, sont bien sûr oxydables, et ne sont pas biodégradables. Si leur élimination n'est pas faite par la voie de l'urine ou autre, elles risquent donc de rester dans l'organisme, et ce, pendant une durée indéterminée. Les effets secondaires sont encore mal connus.
Des chercheurs proposent donc de synthétiser des nanoparticules de fer pur aux propriétés magnétiques innovantes, de développer un nouvel enrobage pouvant les protéger de l'oxydation et d'assurer leur ciblage vers certaines cellules tumorales. Le défi est d'obtenir pour ces nanoparticules une forte sélectivité pour les différentes tumeurs et une grande efficacité préservée tout au long du traitement.