La Puce à Protéines
Les recherches sur les puces à protéines, tout comme les puces à ADN, ont été synonymes de révolution biotechnologique. La petite taille de ces laboratoires sur puce (quelques cm²) permet d’économiser à la fois du temps, mais aussi de l’argent. Les gros appareils étant désormais inutiles. Cet effort a été permis en partie grâce aux travaux combinés de chercheurs, électroniciens, chimistes et informaticiens, notamment sur la protéomique. La protéomique, terme couvrant plusieurs disciplines visant à comprendre et à surveiller les protéines, est un domaine innovateur. Le projet du génome humain a dévoilé un aspect important de la base moléculaire de la vie : l'ADN fabrique l'ARN qui fabrique les protéines. Toutes les protéines humaines sont déterminées par la séquence de nucléotides (bases ADN), qui est maintenant connue avec 99,6% d'exactitude. Après que les scientifiques aient découvert qu'il y avait de petites variations (différences ou absences) dans le contenu des nucléotides présents dans les gènes des gens, il est devenu possible de procéder à des tests génétiques afin de déterminer le profil de l'expression d'une protéine ( profil protéinique ). La mise au point des "profils protéiniques" devrait être plus complexe mais aussi plus efficace que celle des profils ADN ou ARN. Cette nouvelle autre méthode, tout aussi efficace que la première, voire encore plus, va donc permettre d’accomplir de grandes avancées au niveau du diagnostic de certaines maladies. Ce procédé moléculaire appliqué au diagnostic du cancer possède non seulement une sensibilité de détection élevée, mais permet également d’identifier rapidement les agents pathogènes incriminés ainsi que les micro-organismes échappant aux méthodes conventionnelles (techniques classiques avec lesquelles un tel diagnostic n’était pas possible). C’est pourquoi, les puces à protéines deviennent des outils incontournables dans le domaine médical, en particulier, pour le diagnostic et le pronostic des maladies infectieuses (mais aussi auto-immunes et allergiques ).
Le principe de fonctionnement de la puce à protéines est donc fortement similaire à celui de la puce à ADN, la mise en présence de protéines établis sur une plaque de verre et d’autres micro-organismes va entrainer des réactions, suivant lesquelles nous allons diagnostiquer une maladie par étude du séquençage des complexes établis.
La complexité de cette manoeuvre réside dans le grand nombre de protéines de l'organisme (estimé entre 500.000 et 1.000.000). Cela s'explique par le fait que lors de la transcription (passage de l'information génétique de l'ADN à l'ARNm), différentes molécules d'ARNm peuvent être obtenues à partir de la même séquence d'ADN. De plus les protéines peuvent ensuite être modifiées par des réactions chimiques. Le protéome humain n'est donc pas facile à cerner. Les scientifiques recherchent donc une méthode qui permettrait l'analyse en parallèle d'un grand nombre de protéines en s'inspirant du succès des puces à ADN.
Le principe de fonctionnement de la puce à protéines est donc fortement similaire à celui de la puce à ADN, la mise en présence de protéines établis sur une plaque de verre et d’autres micro-organismes va entrainer des réactions, suivant lesquelles nous allons diagnostiquer une maladie par étude du séquençage des complexes établis.
La complexité de cette manoeuvre réside dans le grand nombre de protéines de l'organisme (estimé entre 500.000 et 1.000.000). Cela s'explique par le fait que lors de la transcription (passage de l'information génétique de l'ADN à l'ARNm), différentes molécules d'ARNm peuvent être obtenues à partir de la même séquence d'ADN. De plus les protéines peuvent ensuite être modifiées par des réactions chimiques. Le protéome humain n'est donc pas facile à cerner. Les scientifiques recherchent donc une méthode qui permettrait l'analyse en parallèle d'un grand nombre de protéines en s'inspirant du succès des puces à ADN.
Structure d'une biopuce
Les puces à protéines permettent de détecter des interactions avec différents types de molécules et s’avèrent être un outil puissant pour la compréhension des pathologies humaines, l’évaluation de la réponse immunitaire aux antigènes viraux et bactériens et le développement des méthodes diagnostiques. Dans notre cas, nous allons nous intéresser au diagnostic de maladies telles que le cancer.
Cette technologie, qui est en pleine émergence, possède l’avantage de pouvoir comparer et caractériser simultanément un grand nombre de cibles protéiques (des protéines, des anticorps, des acides nucléiques, des lipides…) tout en remplaçant de nombreux tests individuels (donc gain de temps et d’argent) par un seul et unique test. Cela permettra enfin d’élucider une partie du mystère qui plane autour de la complexité des nombreuses interactions moléculaires à l'échelle de l’organisme. Les informations acquises permettront alors de déterminer les fonctions de chaque protéine ainsi que leur profil d'expression et ainsi détecter celles à la base du cancer. Car rappelons le, le cancer est la conséquence d’une multiplication excessive de certaines cellules, une ou des protéines doivent donc en être la cause. Les protéines sont donc un meilleur reflet du fonctionnement des cellules. Si l’on arrivait à trouver les fonctions précises de chaque protéine et son profil d'expression, nous pourrions déterminer lesquelles sont responsables de cancer et ainsi mieux les cibler pour tenter de les inhiber, donc de guérir le cancer. Mais avant cela, le diagnostic est nécessaire. Ce diagnostic peut-être établie par l’identification de l’agent pathogène incriminé ou d’anticorps spécifiques dirigés contre cet agent. Une fois ces antigènes détectés, le cancer peut-être diagnostiqué. Le répertoire d'antigènes établie par les chercheurs permet de reconnaitre le type de cancer concerné.
Cependant, un certain nombre de difficultés persistent. Les protéines sont des molécules peu stables. Leurs propriétés chimiques dépendent de leur structure, qui se modifie lors de contacts avec des surfaces spécifiques. Les propriétés chimiques des protéines dépendent fortement des séquences d'acides aminés et sont très diverses. Les protéines peuvent être hydrophiles ou hydrophobes, acides ou basiques. Ces caractéristiques impliquent donc que conception de puces à protéines est plus complexe que celle des puces à ADN. Il faut en particulier fabriquer des surfaces sur lesquelles on puisse fixer les protéines sans modifier leur structure pour ne pas modifier leurs propriétés biologiques. Il faut également trouver des molécules réceptrices qui se fixent sur les protéines.
Une puce à protéines est composée d’un arrangement ordonné d’un grand nombre de protéines sur un support miniaturisé, pouvant contenir des protéines actives ou des membres d’une famille de protéines, voire même l’ensemble des protéines d’un organisme (protéome). La technologie comprend trois étapes principales: le dépôt des protéines-cibles sur le support, les interactions cibles-sondes et la détection des
signaux afin d’établir le diagnostic.
Le dépôt
A la différence de la technologie des puces à ADN, l’un des problèmes majeurs rencontré dans la préparation des puces à protéines est le choix du support permettant d’assurer l’arrimage des protéines et le maintien de leur configuration spatiale authentique, condition nécessaire pour évaluer les interactions spécifiques impliquées dans leurs fonctions. Car il faut savoir que les protéines sont très sensibles aux conditions physico-chimiques de leur environnement.
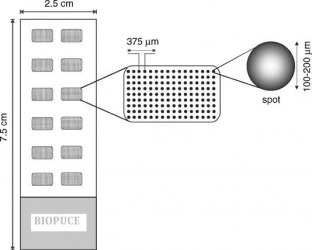
Le dépôt des protéines est effectué à l’aide d’un robot et la miniaturisation du format a permis de préparer des micropuces comprenant 1600 spots de 100 à 200 μm de diamètre par cm², ce qui est quand même énorme. Les protéines étant établies sur une plaque de verre, support inerte et mécaniquement stable, un support qui les immobilisera est donc nécessaire à leur mise en place. Il existe plusieurs méthodes de fixation des protéines sur ces plaques, certaines très complexes, d’autres en pleine amélioration.
Une de ces méthodes consiste à recouvrir la lame de verre d’une couche de polymère telle que le polyacrylamide, l’agarose ou la gélatine, des structures poreuses. Un film de gélose qui renferme de 70% à 95% d’eau permet d’assurer le maintien de la structure tridimensionnelle des protéines immobilisées (qui,rappelons le, doivent rester dan un milieu aqueux) et de mieux les fixer. Cette technique est devenue la plus courante grâce à sa facilité d’utilisation et son efficacité. De plus, grâce à sa surface poreuse, la gélose est capable de maintenir un plus grand nombre de protéines que la plaque de verre.La demi-vie des protéines immobilisées s’étant révélée plus longue dans le milieu gélosique, ce type de puces restent opérationnelles plusieurs mois, donc il n’y a pas de problèmes quant à leur « date de péremption ».
La plaque de verre recouverte de protéines immobilisées est alors prête à l'emploi.
Cette technologie, qui est en pleine émergence, possède l’avantage de pouvoir comparer et caractériser simultanément un grand nombre de cibles protéiques (des protéines, des anticorps, des acides nucléiques, des lipides…) tout en remplaçant de nombreux tests individuels (donc gain de temps et d’argent) par un seul et unique test. Cela permettra enfin d’élucider une partie du mystère qui plane autour de la complexité des nombreuses interactions moléculaires à l'échelle de l’organisme. Les informations acquises permettront alors de déterminer les fonctions de chaque protéine ainsi que leur profil d'expression et ainsi détecter celles à la base du cancer. Car rappelons le, le cancer est la conséquence d’une multiplication excessive de certaines cellules, une ou des protéines doivent donc en être la cause. Les protéines sont donc un meilleur reflet du fonctionnement des cellules. Si l’on arrivait à trouver les fonctions précises de chaque protéine et son profil d'expression, nous pourrions déterminer lesquelles sont responsables de cancer et ainsi mieux les cibler pour tenter de les inhiber, donc de guérir le cancer. Mais avant cela, le diagnostic est nécessaire. Ce diagnostic peut-être établie par l’identification de l’agent pathogène incriminé ou d’anticorps spécifiques dirigés contre cet agent. Une fois ces antigènes détectés, le cancer peut-être diagnostiqué. Le répertoire d'antigènes établie par les chercheurs permet de reconnaitre le type de cancer concerné.
Cependant, un certain nombre de difficultés persistent. Les protéines sont des molécules peu stables. Leurs propriétés chimiques dépendent de leur structure, qui se modifie lors de contacts avec des surfaces spécifiques. Les propriétés chimiques des protéines dépendent fortement des séquences d'acides aminés et sont très diverses. Les protéines peuvent être hydrophiles ou hydrophobes, acides ou basiques. Ces caractéristiques impliquent donc que conception de puces à protéines est plus complexe que celle des puces à ADN. Il faut en particulier fabriquer des surfaces sur lesquelles on puisse fixer les protéines sans modifier leur structure pour ne pas modifier leurs propriétés biologiques. Il faut également trouver des molécules réceptrices qui se fixent sur les protéines.
Une puce à protéines est composée d’un arrangement ordonné d’un grand nombre de protéines sur un support miniaturisé, pouvant contenir des protéines actives ou des membres d’une famille de protéines, voire même l’ensemble des protéines d’un organisme (protéome). La technologie comprend trois étapes principales: le dépôt des protéines-cibles sur le support, les interactions cibles-sondes et la détection des
signaux afin d’établir le diagnostic.
Le dépôt
A la différence de la technologie des puces à ADN, l’un des problèmes majeurs rencontré dans la préparation des puces à protéines est le choix du support permettant d’assurer l’arrimage des protéines et le maintien de leur configuration spatiale authentique, condition nécessaire pour évaluer les interactions spécifiques impliquées dans leurs fonctions. Car il faut savoir que les protéines sont très sensibles aux conditions physico-chimiques de leur environnement.
Le dépôt des protéines est effectué à l’aide d’un robot et la miniaturisation du format a permis de préparer des micropuces comprenant 1600 spots de 100 à 200 μm de diamètre par cm², ce qui est quand même énorme. Les protéines étant établies sur une plaque de verre, support inerte et mécaniquement stable, un support qui les immobilisera est donc nécessaire à leur mise en place. Il existe plusieurs méthodes de fixation des protéines sur ces plaques, certaines très complexes, d’autres en pleine amélioration.
Une de ces méthodes consiste à recouvrir la lame de verre d’une couche de polymère telle que le polyacrylamide, l’agarose ou la gélatine, des structures poreuses. Un film de gélose qui renferme de 70% à 95% d’eau permet d’assurer le maintien de la structure tridimensionnelle des protéines immobilisées (qui,rappelons le, doivent rester dan un milieu aqueux) et de mieux les fixer. Cette technique est devenue la plus courante grâce à sa facilité d’utilisation et son efficacité. De plus, grâce à sa surface poreuse, la gélose est capable de maintenir un plus grand nombre de protéines que la plaque de verre.La demi-vie des protéines immobilisées s’étant révélée plus longue dans le milieu gélosique, ce type de puces restent opérationnelles plusieurs mois, donc il n’y a pas de problèmes quant à leur « date de péremption ».
La plaque de verre recouverte de protéines immobilisées est alors prête à l'emploi.
Les interactions
Le diagnostic du cancer va être effectué à l'aide des marqueurs diagnostiques. Ces marqueurs sont spécifiques, en effet, ce sont des anticorps que l'organisme va synthétiser pour contrer les agents pathogènes du cancer. Ainsi, dès que le cancer se développera dans l'organisme, la concentration d'anticorps spécifiques, augmentera sensiblement dans le corps. En détectant cette concentration, les chercheurs sont capables de déterminer à quel type de cancer on a à faire.
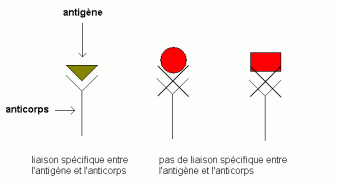
Tout d'abord, les anticorps sont prélevés à partir du sérum ( urine, sang ) du patient. Ensuite ces anticorps (qui sont des protéines) seront déposés sur la puce à protéine, comme nous l'avons expliqué plus haut, puis mis en présence d'antigènes (qui sont aussi des protéines associées à des molécules) spécifiques. Ces antigènes sont caractéristiques de tel ou tel cancer, c'est d'ailleurs de cette façon que l'on arrive à déterminer la nature du cancer. Les interactions protéiques qui auront lieu entre ces anticorps et ces antigènes vont permettre de diagnostiquer la maladie. En effet, si aucun complexe n'est formé, cela veut dire que la maladie caractérisée par les antigènes en question n'est pas déclarée. Mais si au contraire on observe la formation de complexes, cela veut dire qu'il y a affinité entre les anticorps et les antigènes, ce qui révèle la présence d'anticorps produits pour contrer les antigènes introduits, autrement dit les anticorps contre le cancer (voir image). La cancer est alors diagnostiqué. Il s'agit donc de quantifier une protéine précise de ce cancer. On appelle ces puces "puces analytiques".
D'autres interactions ont lieu entre les protéines cibles et les protéines afin de déterminer le profil d'expression de ces dernières. En effet, en associant un agent fluorescent à ces protéines, on arrive à déterminer quelle protéine est sur exprimée ou sous exprimée, c'est le même principe que pour les puces à ADN. Cela permet, par comparaison à des protéines saines, de déterminer très précisément quelle protéine est défaillante, et donc de détecter la cause du cancer. Ces puces sont appelées "puces fonctionnelles".
Détection
Pour la détection le principe est le même que pour les puces à ADN. Avant le dépôt des protéines, un fluorophore ( Cy3 ou Cy5 ) est associé aux sondes et aux cibles, de couleur différente biensur. Une fois les protéines mises en contact, les complexes formés émettront une fluorescence détectable. La lecture des spots sera alors réalisée par un logiciel qui va analyser cette fluorescence et traduire les informations sous forme de couleurs. Ainsi, nous obtiendrons des points de couleur représentatifs de l'expression des protéines. Si la couleur est trop prononcée, cela voudra dire que la protéine étudiée est sur exprimée ou sous exprimée, donc anormale. En fonction de cette expression, les chercheurs peuvent déterminer la nature du cancer, et surtout son pronostic.
Tout d'abord, les anticorps sont prélevés à partir du sérum ( urine, sang ) du patient. Ensuite ces anticorps (qui sont des protéines) seront déposés sur la puce à protéine, comme nous l'avons expliqué plus haut, puis mis en présence d'antigènes (qui sont aussi des protéines associées à des molécules) spécifiques. Ces antigènes sont caractéristiques de tel ou tel cancer, c'est d'ailleurs de cette façon que l'on arrive à déterminer la nature du cancer. Les interactions protéiques qui auront lieu entre ces anticorps et ces antigènes vont permettre de diagnostiquer la maladie. En effet, si aucun complexe n'est formé, cela veut dire que la maladie caractérisée par les antigènes en question n'est pas déclarée. Mais si au contraire on observe la formation de complexes, cela veut dire qu'il y a affinité entre les anticorps et les antigènes, ce qui révèle la présence d'anticorps produits pour contrer les antigènes introduits, autrement dit les anticorps contre le cancer (voir image). La cancer est alors diagnostiqué. Il s'agit donc de quantifier une protéine précise de ce cancer. On appelle ces puces "puces analytiques".
D'autres interactions ont lieu entre les protéines cibles et les protéines afin de déterminer le profil d'expression de ces dernières. En effet, en associant un agent fluorescent à ces protéines, on arrive à déterminer quelle protéine est sur exprimée ou sous exprimée, c'est le même principe que pour les puces à ADN. Cela permet, par comparaison à des protéines saines, de déterminer très précisément quelle protéine est défaillante, et donc de détecter la cause du cancer. Ces puces sont appelées "puces fonctionnelles".
Détection
Pour la détection le principe est le même que pour les puces à ADN. Avant le dépôt des protéines, un fluorophore ( Cy3 ou Cy5 ) est associé aux sondes et aux cibles, de couleur différente biensur. Une fois les protéines mises en contact, les complexes formés émettront une fluorescence détectable. La lecture des spots sera alors réalisée par un logiciel qui va analyser cette fluorescence et traduire les informations sous forme de couleurs. Ainsi, nous obtiendrons des points de couleur représentatifs de l'expression des protéines. Si la couleur est trop prononcée, cela voudra dire que la protéine étudiée est sur exprimée ou sous exprimée, donc anormale. En fonction de cette expression, les chercheurs peuvent déterminer la nature du cancer, et surtout son pronostic.
Le principe reste donc similaire à celui de la puce à ADN, sauf que dans ce cas, là ou les puces à ADN permettent de déterminer la présence d'un gène, la puce à protéines va faire mieux et va mettre en évidence l'expression du gène. Cette méthode serait ainsi plus précise car nous savons précisément quelle entité est à l'origine du dysfonctionnement qu'est le cancer.
Les puces à protéines constituent donc un outil puissant et efficace qui va permettre de diagnostiquer le cancer par comparaison de l'expression d'une protéine cancéreuse et une protéine saine. Il reste cependant un certain nombre de difficultés à surpasser afin de faciliter la conception des puces à protéines. Les chercheurs travaillent d'arrache-pied pour tenter de palier à ces problèmes de la manière la plus naturelle, et la plus simple possible, et les résultats de leurs recherches sont encourageants.
La précision apporté par ce dispositif risque de révolutionner la recherche pour le cancer. Ces nouvelles technologies ne cessent d'être perfectionnées, et nous espérons, dans un futur proche, pouvoir mettre fin à cette domination du cancer que l'être humain est en train de subir.

