Des Nano-Vecteurs efficaces
Nous avons vu que les techniques actuelles de thérapie du cancer ne sont pas toujours très efficace. La chimiothérapie, par exemple, peut détruire des cellules saines et le contrôle des quantités injectés n'est pas encore très bien contrôlé. La bionanotechnologie nous propos donc un nouveau procédé : la vectorisation à l'aide des nanoparticules. La vectorisation est un phénomène qui consiste à administrer des médicaments directement à la cellule malade afin d’éviter aux cellules saines d'être affectées par ce médicament. Cette recherche s'appuie sur de nouveaux concepts physico-chimiques, étant donné qu'il est beaucoup question d'étudier les interactions entre les différentes molécules d'une cellule. Nous assistons donc à une véritable révolution dans le domaine de la "nano-chimiothérapie". Le gros avantage est donc que l'on peut cibler chaque cellule, et surtout doser la quantité de médicament à administrer. Les nanoparticules sont particulièrement efficaces pour administrer les médicaments. Sous diverses formes, elles peuvent en contenir les principes actifs. La petite taille et la biocompatibilité de ces dispositifs thérapeutiques les font aisément pénétrer dans l'organisme. La nanoparticule va donc servir de vecteur, son rôle est de protéger la molécule thérapeutique des attaques causées par les anticorps humains mais aussi de cibler l’endroit où cette molécule ira se fixer.
Vectoriser un médicament, c'est utiliser un support nommé "vecteur" pour l'acheminer sur le site malade dans un but thérapeutique. Il va donc de soit que cette vectorisation doit s'opérer sans altérer les organes sains ou l'équilibre physiologique du patient. La vectorisation des médicaments fait l'objet de nombreuses recherches impliquant différentes approches car elle concerne pratiquement toutes les maladies et plus particulièrement celles qui accablent l'Humanité, comme le cancer.
On peut dire que les nanoparticules sont des vecteurs efficaces car leur index thérapeutique (capacité à traiter une maladie) est élevé par rapport aux techniques conventionnelles. Cela est du au fait que l'utilisation des nanoparticules va permettre dans un premier temps de cibler les cellules malades, donc de n'incorporer que la dose qu'il faut, et dans un deuxième temps, leur grande surface par rapport à leur volume va permettre d'administrer plus de principe actif, il n'y aura donc pas besoin d'injecter une grande quantité de ces vecteurs dans le sang ce qui implique une baisse des risques liés à la toxicité.
On peut dire que les nanoparticules sont des vecteurs efficaces car leur index thérapeutique (capacité à traiter une maladie) est élevé par rapport aux techniques conventionnelles. Cela est du au fait que l'utilisation des nanoparticules va permettre dans un premier temps de cibler les cellules malades, donc de n'incorporer que la dose qu'il faut, et dans un deuxième temps, leur grande surface par rapport à leur volume va permettre d'administrer plus de principe actif, il n'y aura donc pas besoin d'injecter une grande quantité de ces vecteurs dans le sang ce qui implique une baisse des risques liés à la toxicité.
Il existe plusieurs types de vecteurs, de différentes générations, mais qui agissent tous de la même façon. En effet, il s'agit d'abord de fonctionnaliser le vecteur, c'est à dire lui intégrer un agent qui va lui permettre de reconnaitre la cellule cible. Le vecteur sera ensuite injecté dans l'organisme par voie intraveineuse afin de rejoindre la cellule malade. A ce niveau là, le mode d'action des différents types de vecteurs varie. Rappelons que l'environnement d'une cellule cancéreuse, ou plus globalement d'une tumeur, est différent de celui des cellules saines. En effet, on remarque que le Ph du milieu cellulaire d'une métastase par exemple varie entre 5.5 et 6.5 tandis que celui des cellules saines stagne à 7.4 environ. De plus, les cellules cancéreuses possèdent de nombreux marqueurs biologiques qui nous permettent de les repérer, dans notre cas, retenons les récepteurs de l'acide folique (ou vitamine B9). Et pour finir, il faut savoir que les vaisseaux sanguins qui irriguent ces cellules cancéreuses sont beaucoup plus poreuses que ceux des cellules saines. Ces particularités servent à mieux cibler les tumeurs à l'aide des différents types de vecteurs.
On distingue trois types de vecteurs :
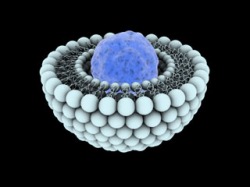
- le liposome, vésicule biodégradable composée deux couche de lipides et d'un compartiment aqueux au centre de la nanoparticule. Lorsque le principe actif du médicament à stocker sans le liposomes est hydrophile, il est placé dans le compartiment aqueux, mais lorsqu'il est lipophile, il est placé dans la bicouche de lipides.
Le liposome mesure environ 100nm ce qui fait de lui un agent 70 fois plus petit qu'une globule rouge.
- la nanosphère, polymère ( molécules enchevêtrés) biodégradable de forme sphérique . Le principe actif du médicament est dispersé dans la matrice de polymère. Ce principe actif sera libéré lors de la dégradation de la nanosphère (lors de l'endocytose).
- la nanocapsule, paroi fine de polymère biodégradable qui entoure le principe actif. On parle alors de "réservoir" du principe actif.
Nous allons caractériser et expliquer le mode de fonctionnement des trois principales générations d'un type de vecteur précis : les liposomes.
Liposome : 1ère génération
Les liposomes de 1ère génération ne contiennent que le principe actif, sans autres substances. L'injection par la voie intraveineuse des liposomes dans le système sanguin entraine une réaction de la part des anticorps, qui détectent ce corps étranger et le marquent comme étant du "non moi" à l'aide de l'opsonine (protéine) via des interactions hydrophobes fortes. Ce marquage va permettre aux macrophages (ou cellules de Kupffer) de reconnaitre ce liposome exogène et de l'internaliser, grâce aux récepteurs opsoniens qu'ils possèdent. Les liposomes sont alors détruits, libérant le principe actif du médicament dans le macrophage. En fonction de ses caractéristiques physico-chimiques, le principe actif diffuse à travers la membrane plasmique du macrophage. Il pourra alors atteindre les cellules hépatiques malades. Les macrophages étant des anticorps du foie, le cancer ainsi que plusieurs maladie du foie peuvent être soignés avec beaucoup d'efficacité. On parle alors de zone prédisposée à être soignée. Le ciblage est ici permis grâce à l'action des cellules de Kupffer qui vont servir de transporteurs.
Liposome pégylé : 2ème génération

Le liposome de 2ème génération est lui, composé du principe actif en plus de polyéthylène glycol ou PEG (ou macrogol), d'ou le nom "pégylé". Le PEG étant un polymère hydrophile (et très soluble), l'opsonisation par interactions hydrophobes n'aura pas lieu car les protéines ne peuvent plus absorber la nanoparticule (il y a répulsion stérique), ce qui va permettre à cette génération de liposomes d'être furtive. Le but est ici de tromper les anticorps pour passer cette première barrière de notre organisme. Ces liposomes peuvent donc circuler dans le système vasculaire. Les macrophages ne pourront pas les reconnaitre, car non opsonisés, ce qui leur permettra d'atteindre des organes cancéreux. L'acheminement jusque ces organes est permis par la porosité de leurs capillaires, en effet, un organe maladie comprend une "tuyauterie" qui comporte des "trous" comme nous l'avons vu plus haut. Cela va donc faciliter et favoriser le passage des liposomes de 2ème génération dans les cellules cancéreuses. L'internalisation qui suivra permettra de dégrader le liposome, et donc de libérer le principe actif dans la cellule malade.
Le ciblage est donc, dans ce cas, permis par les caractéristiques spécifiques qu'acquiert l'endothélium vasculaire (couche interne des vaisseaux sanguins) des organes cancéreux.
Le ciblage est donc, dans ce cas, permis par les caractéristiques spécifiques qu'acquiert l'endothélium vasculaire (couche interne des vaisseaux sanguins) des organes cancéreux.
Liposome pégylé et décoré : 3ème génération

Les liposomes de 3ème génération sont composés du principe actif auquel se rajoutent le PEG et des récepteurs aux marqueurs biologiques du cancer. Ces récepteurs vont par la suite permettre de cibler les cellules cancéreuses. Ce sont donc des liposomes de 2ème génération "décorés" de récepteurs. Cette 3ème génération de liposomes est considérée comme le nec plus ultra des liposomes, car ce sont les vecteurs idéale à la vectorisation d'un médicament. Le récepteur le plus utilisé est l'acide folique (ou vitamine B9) qui va permettre d'établir une interaction avec une molécule spécifique hyperexprimée d'un certain nombre de cancers. On parle alors d'adressage moléculaire, on met en présence une particule avec une substance spécifique pour cibler une cellule. Le PEG permettra de passer les barrières des anticorps, et lorsque le liposome de retrouvera dans le système vasculaire. En arrivant à proximité d’un tissu tumoral, le liposomes pégylé et décoré rencontre un épithélium (tissu de l'organisme) vasculaire discontinu (poreux). Il va alors pouvoir diffuser passivement au travers de l’épithélium vasculaire et atteindre la tumeur. L'acide folique va permettre d'annexé les cellules tumorales qui vont internaliser le liposome et donc le détruire, ce qui va permettre au médicament d'être dispersé. La cellule est ainsi tuée ou soignée.
On parle donc de ciblage de cellules cancéreuses.
On parle donc de ciblage de cellules cancéreuses.
La vectorisation des médicaments par le biais des nanoparticules est donc aujourd'hui l'une des meilleurs méthodes pour venir à bout du cancer. Des nanovecteurs de plus en plus élaborés apparaissent et permettent de contourner les problèmes rencontrés à chaque génération de vecteurs. Ce domaine est en pleine ébullition les recherches ne cessent de donner des résultats et l'étude des caractéristiques des cellules cancéreuses bat son plein. La fonction de ces vecteurs ne se limitent pas qu'à la vectorisation des médicaments, en effet, les nanovecteurs sont aussi utilisés dans la thérapie génique afin d'acheminer le gène sain jusqu'au noyau de la cellule défectueuse, des modification sont biensur apportées afin de passer d'autres barrières de l'organisme.
Aujourd'hui, des liposomes de 2ème génération sont déjà commercialisés en Europe et les analystes prévoient une véritable explosion du marché des nanovecteurs dans les année à venir.
Aujourd'hui, des liposomes de 2ème génération sont déjà commercialisés en Europe et les analystes prévoient une véritable explosion du marché des nanovecteurs dans les année à venir.
